核准日期:
依达拉奉注射液说明书
请仔细阅读说明书并在医师指导下使用
【药品名称】
通用名称:依达拉奉注射液
商品名称:瑞迪卡®,RADICUT®
英文名称:Edaravone Injection
汉语拼音:Yidalafeng Zhusheye
【成份】
活性成份:依达拉奉
化学名称:3-甲基-1-苯基-2-吡唑啉-5-酮
化学结构式:
|
|
分子式:C10H10N2O
分子量:174.20
辅料:亚硫酸氢钠、L-半胱氨酸盐酸盐一水合物、氯化钠、氢氧化钠、磷酸。
【性状】
本品为无色的澄明液体。
【适应症】
抑制肌萎缩侧索硬化(ALS)所致功能障碍的进展。
【规格】
100ml:30mg
【用法用量】
通常,成人每日一次,每次60 mg(2袋),静脉滴注60分钟。
通常,将本品的给药期与停药期进行组合以28天为一个疗程,重复此疗程。第1疗程在每日连续给药14天的给药期后停药14天,第2疗程以后在14天中给药10天的给药期后停药14天。
【不良反应】
肌萎缩侧索硬化(ALS)
日本临床试验
在总计317例病例中报告了37例(11.7%)46件不良反应。主要不良反应为皮疹4件(1.3%)、肝功能障碍4件(1.3%)、高血压3件(0.9%)、γ-GTP升高3件(0.9%)、尿葡萄糖阳性3件(0.9%)等。
(1)严重不良反应
1)*急性肾功能不全(0.26%)、肾病综合征(0.02%):可出现急性肾功能不全、肾病综合征,应频繁进行肾功能检查,予以充分的观察。发现肾功能下降表现或少尿等症状时,应中止给药,进行妥善的处置。(参见“【注意事项】的2.重要的基本注意事项“)
2)*急性重型肝炎(发生率不明)、肝功能障碍(0.24%)、黄疸(发生率不明):可出现急性重型肝炎等严重的肝炎、伴有AST(GOT),ALT(GPT),ALP,γ-GTP,LDH,胆红素等显著升高的肝功能障碍、黄疸,应频繁进行肝功能检查,予以充分的观察。发现异常时,应中止给药,进行妥善的处置。(参见“【注意事项】的2.重要的基本注意事项“)
3)血小板减少(0.08%)、粒细胞减少(发生率不明):可发生血小板减少、粒细胞减少,应频繁进行血液检查,予以充分的观察。当发现异常时,应中止给药,进行妥善的处置。(参见“【注意事项】的2.重要的基本注意事项“)
4)弥散性血管内凝血综合征(DIC)(0.08%):可出现弥散性血管内凝血综合征,应定期进行血液学检查。当出现疑似弥散性血管内凝血综合征的血液学表现时,应中止给药,进行妥善的处置。
5)急性肺损伤(发生率不明):可出现伴发热、咳嗽、呼吸困难、胸部X线异常的急性肺损伤,应充分观察患者的状态,出现上述症状时,应中止给药,给予肾上腺皮质激素类药物等妥善的处置。
6)横纹肌溶解(发生率不明):可出现横纹肌溶解,应进行充分观察,当发现肌痛、乏力、CK(CPK)升高、血和尿的肌红蛋白升高时,应中止给药,进行妥善的处置。
7)休克、过敏性反应(发生率均不明):可出现休克、过敏性反应(荨麻疹、血压降低、呼吸困难等),应进行充分观察,当发现异常时,应中止给药,进行妥善的处置。
(2)其他不良反应
|
种类 |
0.1至<5% |
<0.1% |
发生率不明 |
|
过敏症注)* |
皮疹 |
潮红、肿胀, 疱疹、瘙痒感 |
红斑(多形渗出性红斑等) |
|
血液 |
红细胞减少、白细胞增多、白细胞减少、红细胞压积值减少、血红蛋白减少、血小板增加、血小板减少 |
||
|
注射部位* |
注射部位皮疹、注射部位发红、肿胀 |
||
|
肝脏* |
总胆红素升高、尿胆原阳性、AST(GOT)升高、ALT(GPT)升高、LDH升高、ALP升高、γ-GTP升高 |
胆红素尿 |
|
|
肾脏* |
BUN升高、血清尿酸升高、蛋白尿、血尿、肌酐升高 |
血清尿酸降低 |
多尿 |
|
消化系统* |
恶心、呕吐 |
||
|
其他* |
发热、血清胆固醇升高、甘油三酯升高、血清总蛋白减少、CK(CPK)升高、CK(CPK)降低、血清钾降低、血清钾升高、尿葡萄糖阳性 |
热感、血压升高、血清胆固醇降低、血清钙降低、头痛 |
*发生率是根据脑梗死急性期患者的临床试验、批准后调查结果和肌萎缩侧索硬化(ALS)患者的临床试验计算得出。
注)此情况下应采取中止给药等措施进行妥善的处理。
【禁忌】
(1)严重肾功能障碍的患者 [有致肾功能障碍恶化的风险。患者用药参见【注意事项】的2-(3)]。
(2)对本品成分有既往过敏史的患者。
【注意事项】
1. 慎重用药(以下患者应慎用本品)
(1)肾功能障碍、脱水患者[可致急性肾功能不全或肾功能障碍恶化。特别是在给药前BUN/肌酐比值较高的患者中已有多例致命性事件的报告。(参见“2
.重要的基本注意事项“)]
(2)感染患者[全身状态的恶化可导致急性肾功能不全或肾功能障碍恶化。(参见“2.重要的基本注意事项“)]
(3)肝功能障碍患者[有肝功能障碍恶化的风险。(参见“2.重要的基本注意事项“)]
(4)心脏疾病患者[有心脏疾病恶化的风险,并有发生肾功能障碍的风险。]
(5)重度意识障碍(Japan Coma Scale 100以上:施加刺激后仍无法唤醒)患者[已有较多发生致命性事件的报告。(参见“2.重要的基本注意事项“)]
(6)老年人[已有较多致命性事件的报告。(参见“2.重要的基本注意事项“)]
2. 重要的基本注意事项
(1)应在对本品具有充分了解和适应症治疗经验的医生指导下进行给药。
(2)在给药时应向患者或患者代理人充分说明本品的不良反应等信息。
(3)可发生急性肾功能不全或肾功能障碍恶化、严重肝功能障碍、弥散性血管内凝血(DIC),导致致命性的后果。在这些病例中有同时出现肾功能障碍、肝功能障碍、血液障碍等危重病例的报告。
1) 由于检查值的急剧恶化多见于开始给药初期,故应在给药前或开始给药后尽快进行BUN、肌酐、AST(GOT)、ALT(GPT)、LDH、CK(CPK)、红细胞、血小板等肾功能检查、肝功能检查及血液学检查。在本品给药过程中也应频繁进行肾功能检查、肝功能检查和血液学检查,发现检查值出现异常或少尿等表现时,应立即中止给药,进行妥善的处置。在给药后也应继续进行充分的观察。
2) 在给药前BUN/肌酐比值较高等脱水状态的患者中,已有较多致命性事件的报告,在给药时应彻底进行全身管理。
3) 对于肌萎缩侧索硬化(ALS)患者,随着病情的进展,肌萎缩可能伴有血清肌酐值的降低,因此不应将单个时间点的血清肌酐值与基准值进行比较,而应确定血清肌酐值的变化经过,确认有无恶化的趋势。此外,由于BUN值可随体内含水量等因素发生变化,因此不应将单个时间点的BUN值与基准值进行比较,而应确认BUN值的变化经过,确认有无恶化的趋势。
4)
对于肌萎缩患者,在给药开始前和给药期间应定期在测定血清肌酐值/BUN值的基础上增加以血清胱抑素C估算肾小球滤过率和以蓄尿计算肌酐清除率等检查,进行不易受肌肉量影响的肾功能评价。
5) 在给药过程中出现肾功能障碍时,应立即中止给药,在有丰富治疗知识和经验的医生指导下进行妥善的处置。
6) 在给药过程中出现感染等并发症需要合并使用抗生素时,应慎重考虑是否可以继续给药,继续给药时应特别注意进行频繁的检查。此外,给药结束后也应进行频繁的检查予以充分的观察。(参见【药物相互作用】)
7) 在合并感染的患者、重度意识障碍(Japan Coma Scale 100以上)患者中有较多导致致命性事件的报告,所以在给药时应充分考虑风险和获益。
8) 特别在老年人中,已有较多致命性事件的报告,应予以注意。
3. 保管和使用注意事项
(1)为保持制剂的稳定性,包装系统内配有氧气吸收剂,使用前请勿打开塑料袋的次级包装。如次级包装开封,应在24小时内使用。
(2)当次级包装内配置的氧气指示剂颜色变成粉色以外的颜色时不可使用。
(3)避免与高能量的输液、氨基酸制剂混合或经同一途径滴注(混合后可导致依达拉奉浓度降低)。
(4)避免与抗痉挛药注射液(地西泮、苯妥英钠等)混合(可产生白色浑浊)。
(5)避免与坎利酸钾混合(可产生白色浑浊)。
4. 其他注意事项
在犬24小时连续静脉输注的28天给药毒性试验中,当剂量>60 mg/kg/天时可见四肢活动受限、步态异常等症状以及组织病理学检查所见的末梢神经和脊髓(背索)神经纤维变性。
【孕妇及哺乳期妇女用药】
(1)妊娠期或有妊娠可能性的女性尽量不使用本品(尚不清楚妊娠期用药的安全性)。
(2)哺乳期女性在本品用药期间应禁止哺乳(在动物试验(大鼠)中有本品可向乳汁分布的报告)。
【儿童用药】
尚未确定儿童用药的安全性(ALS:无用药经验)。
【老年用药】
通常,老年人的生理功能有所降低,当出现不良反应时,应中止给药,进行妥善的处置。特别在老年人中已有较多致命性事件的报告,应予以注意。(参见“【注意事项】的2.重要的基本注意事项“)
【药物相互作用】
合并用药注意事项
|
药物名称等 |
临床症状、措施方法 |
机制、危险因素 |
|
抗生素 (头孢唑啉钠、盐酸头孢替安、哌拉西林钠等) |
有致肾功能障碍恶化的风险,合并用药时应频繁进行肾功能检查予以充分的观察。(参见“【注意事项】的2. 重要的基本注意事项“) |
机制尚不明确,但由于本品主要经肾脏排泄,所以与肾排泄型抗生素联合用药时,有增加肾脏负担的可能性。 |
【药物过量】
尚不明确。
【临床试验】
未开展确认本品对生存期影响的试验。
1.安慰剂对照双盲比较试验(第2次验证性试验)
以ALS患者(属于El Escorial修订版Airlie House诊断标准的「确定」或「很可能」、ALS严重程度分类为1级或2级、用力肺活量(%FVC)为80%以上和患病时间<2年)为对象,给予本品60 mg或安慰剂静脉滴注6个疗程※的结果,主要评价项目修订版ALS功能评分量表(ALSFRS-R)的变化量如表1,给药组间具有统计学显著差异。
表1 ALSFRS-R评分变化量
|
给药组 |
评价例数a) |
ALSFRS-R评分b) |
变化量d)e) |
与安慰剂组的比较e) |
||
|
第1疗程 开始给药前 |
最终评价时c) |
组间差异[95%置信区间] |
p值 |
|||
|
安慰剂组 |
66 |
41.9±2.2 |
35.0±5.6 |
-7.50±0.66 |
2.49 [0.99, 3.98] |
0.0013 |
|
本品组 |
68 |
41.9±2.5 |
37.5±5.3 |
-5.01±0.64 |
||
a)第3疗程结束病例(到达给药开始后81天的病例)为评价对象
b)平均值±标准差
c)第6疗程给药结束2周后或中止时(LOCF)
d)调整后平均值±标准误
e)基于以给药组、前观察期ALSFRS-R评分变化量、El Escorial修订版Airlie House诊断标准和年龄为因子的方差分析模型
2.安慰剂对照双盲比较试验(第1次验证性试验)
以ALS患者(属于El Escorial修订版Airlie House诊断标准的「确定」、「很可能」或「很可能–实验室–支持」、ALS严重程度分类为1级或2级、%FVC为70%以上,患病时间<3年)为对象,给予本品60 mg或安慰剂静脉滴注6个疗程※的结果,主要评价项目ALSFRS-R的变化量如表2,在给药组间未见统计学显著差异。
表2 ALSFRS-R评分变化量
|
给药组 |
评价例数a) |
ALSFRS-R评分b) |
变化量d)e) |
与安慰剂组的比较e) |
||
|
第1疗程 开始给药前 |
最终 评价时c) |
组间差异[95%置信区间] |
p值 |
|||
|
安慰剂组 |
99 |
41.1±2.9 |
35.1±7.4 |
-6.35±0.84 |
0.65 [-0.90, 2.19] |
0.4108 |
|
本品组 |
100 |
40.5±3.5 |
35.3±7.1 |
-5.70±0.85 |
||
a)第3疗程结束病例(到达给药开始后81天的病例)为评价对象
b)平均值±标准差
c)第6疗程给药结束2周后或中止时(LOCF)
d)调整后平均值±标准误
e)基于以给药组、前观察期ALSFRS-R评分变化量、初始症状(球症状/四肢症状)和及是否合用利鲁唑为因子的方差分析模型
3.以ALS严重程度分类3级患者为对象的安慰剂对照双盲比较试验
以ALS严重程度分类3级的ALS患者为对象,给予本品60 mg或安慰剂静脉滴注6个疗程※的结果,主要评价项目ALSFRS-R的变化量如表3,给药组间不具有统计学显著差异。
表3 ALSFRS-R评分变化量
|
给药组 |
评价例数a) |
ALSFRS-R评分b) |
变化量d)e) |
与安慰剂组的比较e) |
||
|
第1疗程 开始给药前 |
最终评价时c) |
组间差异[95%置信区间] |
p值 |
|||
|
安慰剂组 |
12 |
34.6±3.3 |
29.2±4.9 |
-6.00±1.83 |
-0.52 [-5.62, 4.58] |
0.8347 |
|
本品组 |
13 |
32.5±5.5 |
26.6±9.9 |
-6.52±1.78 |
||
a)第3疗程结束病例(到达给药开始后81天的病例)为评价对象
b)平均值±标准差
c)第6疗程给药结束2周后或中止时(LOCF)
d)调整后平均值±标准误
e)基于以给药组和前观察期ALSFRS-R评分变化量为因子的方差分析模型
※
将每日一次连续给药14天和其之后的14天停药期作为第1疗程,第1疗程结束后,将14天中每日一次共计给药10天和其之后的14天停药期构成的疗程重复5次(第2~6疗程)。
【药理毒理】
药理作用
依达拉奉治疗肌萎缩性侧索硬化症(ALS)的作用机制尚不明确。
毒理研究
遗传毒性
依达拉奉Ames试验、体外中国仓鼠肺细胞染色体畸变试验、小鼠体内骨髓微核试验结果均为阴性。
生殖毒性
雄性大鼠于交配前至交配期、雌性大鼠于交配前至妊娠第7天静脉注射给予依达拉奉3、20、200mg/kg,未见对生育力的影响,但是高剂量组大鼠可见动情周期延长、交配率降低。生殖功能的无影响剂量为20mg/kg,按体表面积(mg/m2)计算,相当于人推荐剂量(RHD)60mg的3倍。
妊娠大鼠于器官发生期静脉注射给予依达拉奉3、30、300mg/kg,各剂量均可使胎仔体重降低,高剂量组可见母体毒性、子代体重降低,未见对子代生殖功能的影响。未确定胚胎-胎仔发育毒性的无影响剂量。按mg/m2计算,低剂量3mg/kg低于RHD 60mg。
妊娠兔于器官发生期静脉注射给予依达拉奉3、20、100mg/kg,高剂量组可见与母体毒性相关的胚胎/胎仔死亡。按mg/m2计算,胚胎-胎仔发育毒性的无影响剂量20mg/kg约相当于RHD的6倍。
在两项试验中,妊娠大鼠于妊娠第17天至哺乳期静脉注射给予依达拉奉3、20、200mg/kg,评估对子代的影响。第一项试验中,高剂量时观察到子代死亡,高、中剂量时活动增加。第二项试验中,高剂量时组可见死产、子代死亡率增加,身体发育(阴道张开)迟缓。两项试验中,均未见对子代生殖功能的影响,高、中剂量组可见明显母体毒性。按mg/m2计算,发育毒性的无影响剂量3mg/kg/天低于RHD。
【药代动力学】
参考RADICUT注射液30 mg的药代动力学
1. 血药浓度
对于健康成年男性(5例)和65岁以上健康老年人(5例),本品以0.5 mg/kg的剂量静脉输注30分钟,每日两次,连续输注2天。根据原型药物的血浆浓度变化和首次给药时的原型药物血浆浓度变化计算的参数如下所示。
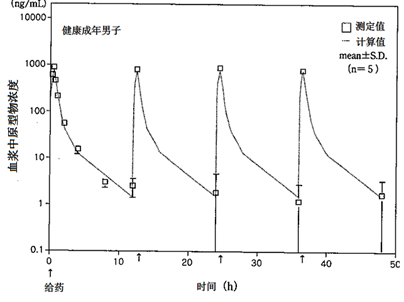

(平均值±S.D.)
|
药代动力学参数 |
健康成年男性 (5例) |
健康老年人 (5例) |
|
Cmax(ng/ml) |
888±171 |
1041±106 |
|
t1/2α(h) |
0.27±0.11 |
0.17±0.03 |
|
t1/2β(h) |
2.27±0.80 |
1.84±0.17 |
健康成年男性和健康老年人的血浆中原型物浓度均以相同的方式消除,未见蓄积。
2. 血清蛋白结合率
依达拉奉(5 μM及10 μM)的人血清蛋白和人血清白蛋白的结合率分别为92%和89-91%(体外)。
3. 代谢
健康成年男性和健康老年人血浆中的主要代谢产物为硫酸盐结合物,也可检测出葡萄糖醛酸结合物。此外,尿液中的主要代谢产物为葡萄糖醛酸结合物,也可见硫酸盐结合物。
4. 排泄
向健康成年男性和健康老年人以每日2次连续2天静脉内给药时(0.5 mg/kg/30分钟×2次/天),在各次给药后12小时内经尿液排泄的原型药物为0.7-0.9%、代谢产物为71.0-79.9%。
【贮藏】
遮光,25℃以下保存。
【包装】
初级包装为聚丙烯袋,次级包装为聚乙烯醇泡罩内含氧气吸收剂和氧气指示剂;100ml/袋,10袋/盒。
【有效期】
36个月
【执行标准】
【进口药品注册证号】
【生产企业】
持证商名称:Mitsubishi Tanabe Pharma Corporation
持证商地址:3-2-10, Dosho-machi, Chuo-ku, Osaka 541-8505, Japan
生产商名称:Terumo Corporation, Kofu Factory
生产商地址:1727-1, Tsuijiarai, Showa-cho, Nakakoma-gun, Yamanashi 409-3853, Japan
